Работа выполнена при поддержке гранта РФФИ №14 03 00417.
Введение. Загрязнение тяжелыми металлами атмосферы, почвы, воды является серьезной проблемой, потому что все больше культурных ландшафтов попадают под их воздействие, что в свою очередь сказывается как на продуктивности сельскохозяйственных культур, так и на качестве продуктов [1,2]. К стойким химическим загрязнителям кумулятивного действия со специфическими токсическими свойствами относятся тяжелые металлы. Значимость проблемы загрязнения окружающей среды тяжелыми металлами объясняется, прежде всего, широким спектром их действия на организм человека. Металлы влияют практически на все системы организма, оказывая токсическое, аллергическое, канцерогенное, гонадотропное действие. Тяжелые металлы и некоторые микроэлементы, находящиеся в повышенных количествах в питьевой воде, влияют на здоровье людей, т.к. обладают тропностью – избирательно накапливаются в определенных органах и тканях, структурно и функционально нарушая их [3,4]. В связи с этим актуальна задача разработки сорбентов, обладающих высокой способностью извлечения ионов металлов из воды и применение которых было бы экономически целесообразно.
Целью данной работы является исследование процесса сорбции ионов тяжелых металлов полисахаридным сорбентом из водных растворов.
Экспериментальная часть. Кинетику сорбции ионов тяжелых металлов исследуют в статических условиях при перемешивании методом ограниченного объема раствора [5]. Для получения кинетических кривых в серию пробирок помещают навески сорбента массой по 0,10 г, заливают их 10 см3 водного раствора сульфата металла. Начальная концентрация ионов металлов составляла 1,5·10-4 моль/л. Через определенные промежутки времени раствор отделяют от сорбента фильтрованием и определяют в нем текущую концентрацию ионов металлов (Сτ) методом атомно-абсорбционной спектроскопии на приборах 210VGP и МГА-915МД.
Для исследования влияния концентрации металла в растворе на равновесие в ионообменной системе получают изотермы сорбции. Для получения изотерм процесс сорбции проводят следующим образом: в серию пробирок помещают навески сорбента массой по 0,10 г и заливают их 10 см3 водного раствора сульфата металла с концентрациями металла в интервале 1,510-4 – 510-2 моль/л и выдерживают при перемешивании до установления состояния равновесия (время достижения сорбционного равновесия определяют при исследовании кинетики сорбции). Затем раствор отделяют от сорбента фильтрованием и определяют в нем равновесную концентрацию ионов металла (Се) методом атомно-абсорбционной спектроскопии. Сорбционную емкость сорбента в каждый конкретный момент времени τ рассчитывают по формуле (1):
где Сsorb.– сорбционная емкость, мг/г; С0 – начальная концентрация ионов металла, моль/л; С – концентрация ионов металла в момент времени , моль/л;
m – масса навески сорбента, г; V – объем раствора, см3.
При снятии изотермы сорбции в условиях установившегося равновесия в системе определяют равновесную концентрацию ионов металла в растворе (Се) и рассчитывают равновесную сорбционную емкость:
где Сsorb.,e – равновесная сорбционная емкость, мг/г; Се – равновесная концентрация ионов металла, моль/л.
Степень извлечения α определяют следующим образом:
.gif) (3)
(3)Коэффициент распределения KD рассчитывают как отношение концентрации ионов металла в фазе полимера (Сsorb.) к его содержанию в растворе:
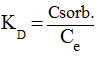 (4)
(4)Биотестирование водной фазы после контакта с сорбентом – топинамбуром проводят с использованием методики, основанной на определении смертности дафний при воздействии токсических веществ, присутствующих в исследуемой водной среде, по сравнению с контрольной культурой в пробах, не содержащих токсических веществ. В качестве тест-объекта используется Daphnia magna Straus. Биотестирование проводят в химических стаканах вместимостью 150 – 200 см3, которые заполняют 100 см3 исследуемой, предварительно насыщенной кислородом воды, в них помещают по десять дафний в возрасте 6 – 24 часа. Учет смертности дафний в опыте и контроле проводят через 24 часа [6].
Результаты и их обсуждение. Для определения параметров, характеризующих сорбционные свойства сорбента из стеблей топинамбура, были получены кинетические кривые сорбции ионов Cu(II), Zn(II). Результаты эксперимента на рисунке 1.
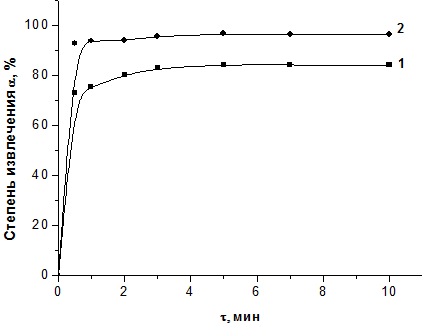
1 – Zn(II); 2 – Cu(II)
Рисунок 1 – Кинетические кривые сорбции ионов тяжелых металлов из водных растворов топинамбуром
Согласно полученным данным стебли топинамбура сравнительно эффективно сорбируют ионы тяжелых металлов. Сорбция ионов Сu(II) выше, чем сорбция ионов Zn(II). Среднее время достижения сорбционного равновесия в гетерогенной системе водный раствор сульфата металла – сорбент составляет 5-10 минут.
Для определения предельной сорбционной емкости топинамбура были получены изотермы сорбции ионов Zn(II) и Cu(II) из водных растворов сульфатов. Результаты эксперимента представлены на рисунке 2.
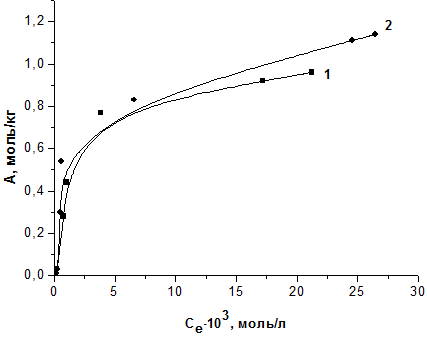
1 – Zn(II); 2 – Cu(II)Рисунок 2 – Изотермы сорбции тяжелых металлов сорбентом из стеблей топинамбура
Полученные экспериментальные данные описаны уравнением изотермы адсорбции Ленгмюра:

где АR – предельная или максимальная сорбционная емкость полимера по данному металлу, моль/кг; К – концентрационная константа сорбционного равновесия, характеризующая интенсивность процесса сорбции, л/моль; Се – равновесная концентрация сорбата, моль/л [7].
Линеаризация изотермы сорбции по уравнению (5) позволяет графически определить в уравнении Ленгмюра величины А и К из опытных данных по распределению исследуемого сорбата в гетерофазной системе водный раствор – целлюлозный сорбент.
.gif)
Результаты обработки изотерм сорбции ионов тяжелых металлов топинамбуром по модели Ленгмюра представлены на рисунке 3 и в таблице 1.
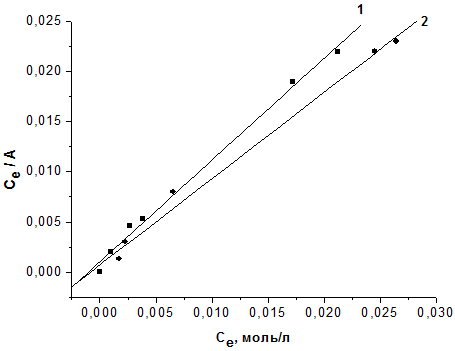
1 – Cu(II); 2 – Zn(II)Рисунок 3 – Обработка изотерм сорбции ионов тяжелых металлов по модели Ленгмюра
Таблица 1 – Параметры обработки изотерм сорбции по модели Ленгмюра методом наименьших квадратов
|
Катион металла
|
1/АК
|
1/А
|
Коэффициент корреляции
|
А, моль/кг
|
|
Cu(II)
|
0,001 ± 510-4
|
0,86 ± 0,04
|
0,99
|
1,16
|
|
Zn(II)
|
0,001 ± 410-4
|
1,02 ± 0,04
|
0,99
|
0,98
|
Однако в последнее время сорбцию различных веществ (неполярных, полярных и ионогенных соединений) на микропористых сорбентах, в том числе, на сорбентах целлюлозной природы, описывают с позиций теории объемного заполнения микропор (ТОЗМ). Согласно литературным данным, большая часть внутреннего пространства целлюлозного волокна приходится на поры диаметром 3 нм, поэтому такие сорбенты можно отнести к твердым адсорбентам с развитой микропористой структурой.
Уравнение ТОЗМ для адсорбции из растворов в его наиболее общей форме имеет вид [7]:
где Е – характеристическая энергия адсорбции, Сs – растворимость сорбата, Се и А – равновесные концентрации распределяемого вещества в объемной и адсорбционной фазах соответственно, А∞ - предельная концентрация сорбата в адсорбционной фазе, n – целое число, преимущественно 1, 2, 3.
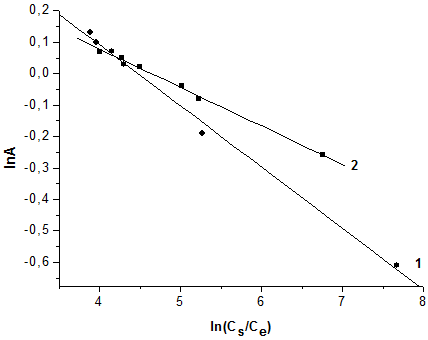
Экспериментальные изотермы были обработаны в рамках модели ТОЗМ (рис. 4).
|
Катион металла
|
lnА∞
|
RT/E
|
Коэффициент корреляции
|
А, моль/кг
|
|
Cu(II)
|
0,86 ± 0,03
|
-0,19 ± 0,01
|
0,99
|
2,36
|
|
Zn(II)
|
0,57 ± 0,02
|
-0,122 ± 0,003
|
0,99
|
1,77
|
Как свидетельствуют литературные данные [8], предельная сорбция (А∞) на немодифицированных целлюлозных сорбентах не превышает 1 моль/кг, а для модифицированных – 2,6 моль/кг. Это согласуется с результатами, полученными при обработке изотермы с использованием модели адсорбции Ленгмюра (табл. 2).
Таким образом, как видно из рис. 3, 4 в координатах Се/А – Се и lnA – ln (Cs/Cе) наблюдаются линейные зависимости с коэффициентом корреляции (R) 0,99. Это говорит о том, что экспериментальные данные по сорбции ионов меди и цинка на топинамбуре хорошо аппроксимируются уравнением Ленгмюра и ТОЗМ, а из значений величин предельной сорбции (А∞) (табл. 1, 2), полученных в ходе обработки изотерм сорбции с использованием этих двух уравнений (моделей сорбции) следует, что данный целлюлозный сорбент обладает достаточно высокой связывающей способности по отношению к ионам меди и цинка.
Выводы. Исследованы сорбционные свойства полисахаридного сорбента из стеблей топинамбура по отношению к ионам Cu(II), Zn(II).
Экспериментальные изотермы сорбции ионов тяжелых металлов обработаны в рамках моделей сорбции Ленгмюра и ТОЗМ. Показано, что модели позволяют достаточно хорошо описывать процесс сорбции с коэффициентом корреляции 0,99 в линейной форме уравнения. Установлено, что предельная сорбция А∞, полученная с использованием модели Ленгмюра согласуется с опытными данными.
Проведена оценка токсичности стеблей топинамбура методом биотестирования по смертности дафний. Установлено, что топинамбур является безопасным и может быть использован для сорбционной очистки пищевых сред.
Библиографический список
- Алексеев Ю.В. Тяжелые металлы в почвах и растениях. Л.: ВО Атомиздат, 1987. 365 с.
- Петров О.Ю., Александров Ю.А. Медико-биологические и нравственные аспекты полноценного питания. Учебное пособие. Йошкар-Ола: ГОУВПО «Марийский государственный университет», 2008. 223 с.
- Когановский А.М. Адсорбция и ионный обмен в процессах водоподготовки и очистки сточных вод. Киев: Наук. думка, 1983. 240 с.
- Теплая Г.А. Тяжелые металлы как фактор загрязнения окружающей среды (Обзор литературы) // Астраханский вестник экологического образования. 2013. № 1 (23). С. 182 – 192.
- Кокотков Ю.А., Пасечник В.А. Равновесие и кинетика ионного бомена. Л.: Химия, 1970. 336 с.
- Григорьев Ю.С., Шашкова Т.Л. Методика определения токсичности водных вытяжек из почв, осадков сточных вод и отходов, питьевой, сточной и природной воды по смертности тест-объекта Daphnia magna Straus (ПНД Ф Т 14.1:2:4.12 – 06; Т 16.1:2.3.3.9 – 06). М.:, 2006. 44 с.
- Фролов Ю. Г. Курс коллоидной химии. Поверхностные явления и дисперсные системы; 2-е изд., перераб. и доп. М.: Химия, 1989. 464 с.
- Целлюоза и ее производные / Под ред. Н. Байклза и Л. Сегала. Пер. с англ. Под ред. докт. техн. наук З.А. Роговина. Т.2. М.: Мир, 1974. 510 с.
