Изучение физико-химических свойств веществ осуществляется на основе лабораторных испытаний. Однако, используя корреляционные графики, выражающие зависимость между топологическими индексами и свойствами веществ, без проведения лабораторных испытаний, изучение свойств веществ является направлением, обладающим широкими перспективами.
Среди топологических индексов, применяемых в сфере изучения свойств химических соединений, можно указать Саркар [1], Раухаудхури [2], Рой [3,4] и др.
Выбор нужного индекса для подробного изучения отдельных свойств является важной задачей. Если при применении какого-либо свойства определенный индекс дает положительные результаты, применение другого индекса не дает возможность для получения точной информации.
Необходимо отметить, что наряду со множеством положительных результатов используемых индексов, в исследованиях, проводимых в различных направлениях, возникают определенные трудности. Примером этому могут служить соединения с различными галогенами в идентичном состоянии одного вещества (C4 H9 F, C4 H9 Cl, C4 H9 Br, C4 H9 J).
Так как атомы элементов в топологических индексах, вычисляемых на основе теории графа, указываются в одинаковых точках, значения, полученные от вычисления топологических индексов веществ с различными галогенами в идентичном состоянии, бывают равными и построение корреляций, выражающих «структура-свойство», становится невозможным.
Проводимые мною исследования в данном направлении дали удачные результаты. Так, новые модификации, полученные прибавлением радиусов различных элементов к вычислению индексов, обеспечили полное решение проблемы.
Информационное содержание графа относительно окрестности к-го порядка (ICk), полного информационного содержания (TICk), структурное информационное содержание (SICk), информационное содержание связывания (BICk) и комплементарное информационное содержание (CICk) (к=0-2) могут быть рассчитаны следующим образом [5]:
![]()
![]() (1)
(1)
![]() (2)
(2)
![]() (3)
(3)
![]() (4)
(4)
![]() (5)
(5)
где n - число вершин графа, равное ![]() , ni – количество вершин в подмножестве i, N - число ребер графа, Ri – радиус атома.
, ni – количество вершин в подмножестве i, N - число ребер графа, Ri – радиус атома.
Топологические индексы ![]() ,
, ![]() , и
, и ![]() химических соединений CH3 X, C2H5X, C3H7X, C4H9X (X>F, Cl, Br, J) даны в следующей таблице.
химических соединений CH3 X, C2H5X, C3H7X, C4H9X (X>F, Cl, Br, J) даны в следующей таблице.
|
Формула
|
|
|
|
|
|
|
|
|
|
|
CH3 F
|
0,0889
|
0,4443
|
2,233
|
0,0889
|
0,4443
|
2,233
|
0,0889
|
0,4443
|
2,233
|
|
CH3Cl
|
0,1051
|
0,52565
|
2,2168
|
0,1051
|
0,52565
|
2,2168
|
0,1051
|
0,52565
|
2,2168
|
|
CH3Br
|
0,1121
|
0,5605
|
2,2098
|
0,1121
|
0,5605
|
2,2098
|
0,1121
|
0,5605
|
2,2098
|
|
CH3J
|
0,1209
|
0,6046
|
2,201
|
0,1209
|
0,6046
|
2,201
|
0,1209
|
0,6046
|
2,201
|
|
C2H5F
|
0,085
|
0,6797
|
2,915
|
0,1042
|
0,8337
|
2,8958
|
0,1364
|
1,091
|
2,8636
|
|
C2H5Cl
|
0,0981
|
0,7847
|
2,9019
|
0,1173
|
0,9387
|
2,8827
|
0,1495
|
1,196
|
2,8505
|
|
C2H5Br
|
0,1037
|
0,8297
|
2,8963
|
0,123
|
0,9837
|
2,877
|
0,1551
|
1,241
|
2,8449
|
|
C2H5J
|
0,1108
|
0,8867
|
2,8892
|
0,1301
|
1,0407
|
2,8699
|
0,1622
|
1,298
|
2,83775
|
|
C3H7F
|
0,0815
|
0,8963
|
3,3779
|
0,1148
|
1,2624
|
3,3447
|
0,1673
|
1,84
|
3,2922
|
|
C3H7Cl
|
0,0925
|
1,0174
|
3,3669
|
0,1258
|
1,3835
|
3,33365
|
0,1783
|
1,961
|
3,28115
|
|
C3H7Br
|
0,0972
|
1,0693
|
3,3622
|
0,1305
|
1,4354
|
3,3289
|
0,183
|
2,013
|
3,2764
|
|
C3H7J
|
0,1032
|
1,135
|
3,3562
|
0,1365
|
1,50115
|
3,323
|
0,189
|
2,0787
|
3,2705
|
|
C4H9F
|
0,0789
|
1,1043
|
3,7285
|
0,1119
|
1,5663
|
3,6955
|
0,175
|
2,4504
|
3,6323
|
|
C4H9Cl
|
0,0884
|
1,2376
|
3,719
|
0,1214
|
1,6996
|
3,686
|
0,1845
|
2,5836
|
3,6228
|
|
C4H9Br
|
0,0925
|
1,2947
|
3,715
|
0,1255
|
1,7567
|
3,6819
|
0,1886
|
2,6408
|
3,6187
|
|
C4H9J
|
0,09765
|
1,3671
|
3,7097
|
0,13065
|
1,8291
|
3,6767
|
0,1938
|
2,7132
|
3,61355
|
Рассмотрим линейные корреляции, выражающие зависимость между плавлением, кипением соединений C2H5X, C3H7X, C4H9X (X>F, Cl, Br, J) с вычисленными индексами.
Температуры плавления и кипения некоторых алкилгалогенидов представлены в таблице-2 [6].
Таблица 2
|
Формула
|
Температура плавления, о С
|
Температура кипения, о С
|
|
C2H5F
|
- 143,2
|
- 37,7
|
|
C2H5Cl
|
- 138,7
|
- 12,2
|
|
C2H5Br
|
- 119
|
38
|
|
C2H5J
|
- 108,5
|
72,2
|
|
C3H7F
|
- 159
|
- 3,2
|
|
C3H7Cl
|
- 122,8
|
47,2
|
|
C3H7Br
|
- 109,8
|
70,9
|
|
C3H7 J
|
- 101,4
|
102,4
|
|
CH3Cl
|
- 97,7
|
- 24,22
|
|
C4H9Cl
|
- 123,1
|
78
|
|
C4H9F
|
- 134
|
32
|
|
C4H9Br
|
- 112,4
|
101,6
|
|
C4H9J
|
- 103,5
|
131
|
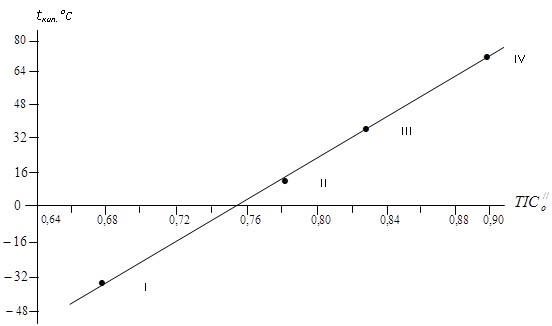
Рис. 1 Корреляция зависимости температуры кипения с топологическим индексом ![]() соединений C2H5F (I), C2H5Cl (II), C2H5Br (III), C2H5J (IV).
соединений C2H5F (I), C2H5Cl (II), C2H5Br (III), C2H5J (IV).
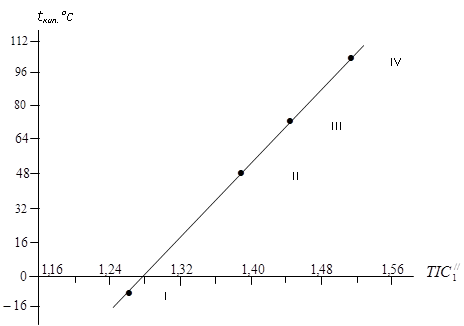
Рис. 2 Корреляция выражающая зависимость температуры кипения с топологическим индексом ![]() алкилгалогенидов C3H7F (I), C3H7Cl (II), C3H7Br(III), C3H7J (IV).
алкилгалогенидов C3H7F (I), C3H7Cl (II), C3H7Br(III), C3H7J (IV).
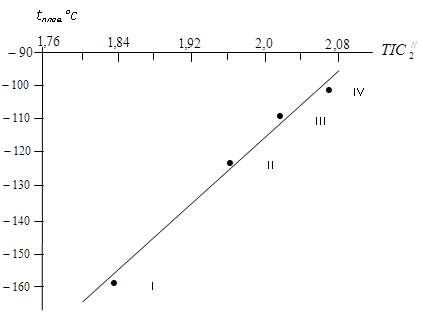
Рис. 3 Корреляция зависимости температуры плавления с топологическим индексом ![]() соединений C3H7F (I), C3H7Cl (II), C3H7Br (III), C3H7J (IV).
соединений C3H7F (I), C3H7Cl (II), C3H7Br (III), C3H7J (IV).
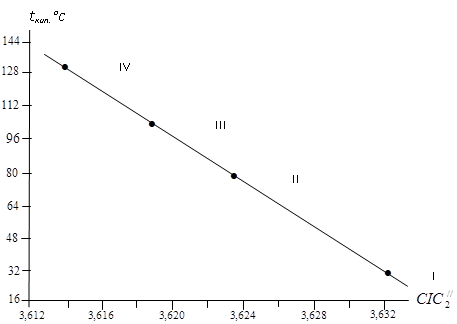
Рис. 4 Корреляция зависимости температуры кипения с топологическим индексом ![]() соединений C4H9F (I), C4H9Cl (II), C4H9Br (III), C4H9J (IV).
соединений C4H9F (I), C4H9Cl (II), C4H9Br (III), C4H9J (IV).
Если применить вновь модифицированные топологические индексы к соединениям с одинаковыми галогенами различных алканов, то получим линейную корреляцию, выражающую связи «структура-свойство».
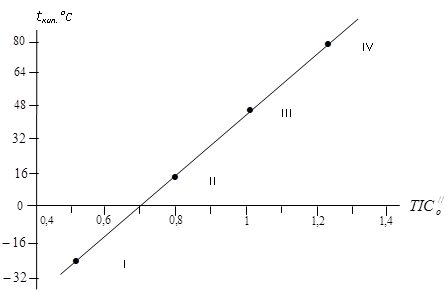
Рис. 5 Корреляция, выражающая зависимость температуры кипения с топологическим индексом ![]() алкилгалогенидов CH3Cl (I), C2H5Cl (II), C3H7Cl(III), C4H9Cl (IV).
алкилгалогенидов CH3Cl (I), C2H5Cl (II), C3H7Cl(III), C4H9Cl (IV).
Наряду с температурами плавления и кипения, построение корреляций, выражающих зависимость между вновь модифицированными топологическими индексами, успешно применяется при изучении неизвестных физико-химических свойств веществ.
Рассмотрим корреляцию, показывающую зависимость между плотностью веществ и топологическими индексами.
Плотности некоторых алкийодидов (![]() ) представлены в нижеследующей таблице.Таблица 3
) представлены в нижеследующей таблице.Таблица 3
| Алкилйодид
плотность |
CH3J
|
C2H5J
|
C3H5J
|
C4H9J
|
| плотность |
2,279
|
1,993
|
1,747
|
1,617
|
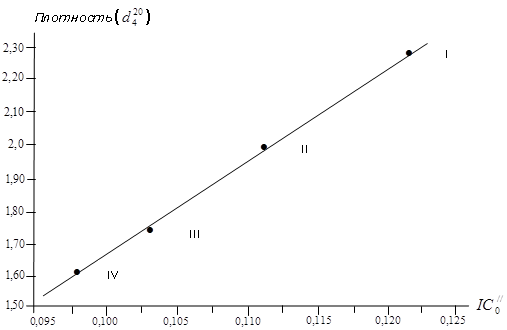
Рис. 6 Корреляция зависимости плотностей (![]() ) с топологическими индексами химических соединений CH3J (I), C2H5J (II), C3H7J (III), C4H9J (IV).
) с топологическими индексами химических соединений CH3J (I), C2H5J (II), C3H7J (III), C4H9J (IV).
Возможно изучение неизвестных свойств веществ с помощью построенных корреляций без проведения лабораторных испытаний. Например, применив топологический индекс ![]() соединения C2H5At к корреляции рис. 1, топологический индекс
соединения C2H5At к корреляции рис. 1, топологический индекс ![]() соединения C3H7At к корреляции рис. 2, топологический индекс
соединения C3H7At к корреляции рис. 2, топологический индекс ![]() соединения C4H9At к корреляции рис. 4, можно определить температуру кипения веществ.
соединения C4H9At к корреляции рис. 4, можно определить температуру кипения веществ.
Применив топологический индекс ![]() соединений C5H11Cl, C6H13Cl и др. к корреляции рис. 5 можно определить температуру кипения веществ.
соединений C5H11Cl, C6H13Cl и др. к корреляции рис. 5 можно определить температуру кипения веществ.
Вычислив математическим путем топологический индекс ![]() веществ C5H11J, C6H13J и др. и применив в рисунку-6 можно найти плотности данных веществ (
веществ C5H11J, C6H13J и др. и применив в рисунку-6 можно найти плотности данных веществ (![]() ).
).
Таким образом, изучение свойств веществ возможно при применении вновь модифицированных индексов, без использования лабораторных испытаний.
Библиографический список
- Sarkar R., Roy A.B., Sarkar P.K., Math. Biosci., 1978, v. 39, p. 299.
- Raychaudhury C., Basak S.C., Ray S.K., Roy A.B., Ghosh J.J., Abstract: 19th Annual Meeting, Society of Engineering Sciences Inc., University of Missouri-Rolla, 1982.
- Roy A.B., Basak S.C., Harriss D.K., Magnuson V.R., In: Proc. of the Fourth Int. Conference on Mathematical Modelling.
- Roy A.B., Raychaudhury C., Ray S.K., Basak S.C., Ghosh J.J., In: Proc. of the Fourth European Symposium on Chemical Structure-Biological Activity: Quantitative Approaches, 1982, p. 75.
- Р.Кинг Химические приложения топологии и теории графов, Москва «Мир» 1987, стр. 213.
- А.Н.Несмеянов, Н.А.Несмеянов. Начала органической химии. Москва 1974, стр. 73.
