Сероводородные газы, образующиеся в процессе очистки углеводородных газов от кислых компонентов, обычно перерабатываются в серную кислоту или элементарную серу. Для утилизации сероводородного газа в элементарную серу обычно применяется хорошо известный в мировой практике процесс Клауса или его различные модификации. В настоящее время почти весь объем промышленного получения серы получается на основе этого процесса. Утилизация серы из перерабатываемой нефти имеет огромное природоохранное значение [1, 2].
Сущность процесса Клауса заключается в переработке сероводородного газа в серу по окислительному методу с применением термической и двух-трех каталитических ступеней [3].
Поступающий на установку Клауса кислый газ подвергается высокотемпературному (900 – 1300°С) сжиганию в свободном пламени в присутствии стехиометрического количества воздуха с получением элементарной серы (выход до 70%) и диоксида серы в соответствии с уравнениями [4]:
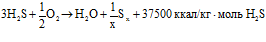 , (1)
, (1)
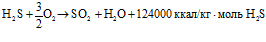 . (2)
. (2)
Принято считать, что при стехиометрическом количестве кислорода в топке часть H2S реагирует по реакции (1), а треть непрореагировавшего H2S – по реакции (2). Поэтому на выходе из топки в газах соотношение H2S/SO2 получается равным 2.
Однако представляется более правильным образование серы через моноокись серы. Тогда механизм пламенного сжигания сероводорода будет выражаться следующими уравнениями:
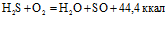 , (3)
, (3)
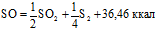 , (4)
, (4)
 , (5)
, (5)
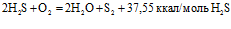
Реакция (3) и (4) протекают с большой скоростью, поэтому выход серы будет лимитироваться скоростью реакции (5).
Получаемый по реакции (2) сернистый ангидрид окисляется на бокситовом катализаторе гидроаргиллитовой структура при температуре 370 – 400°С по реакциям:
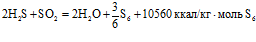 , (6)
, (6)
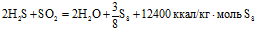 , (7)
, (7)
Реакция идет частично на термической стадии при охлаждении газового потока, но в большем объеме – на стадии каталитического окисления.
Подача воздуха в камеру сгорания ведется с таким расчетом, чтобы на выходе из печи соотношение H2S:SО2 составляло 2:1 (в соответствии с последующей реакцией каталитического окисления сероводорода диоксидом серы). Содержание кислорода в отходящих газах должно быть сведено к минимуму, так как его наличие способствует сульфатации катализатора на основе оксида алюминия.
На всех стадиях процесса степень превращения сероводорода стремятся довести до состояния термодинамического равновесия. Равновесная конверсия сероводорода в серу в интервале температур 150 ÷ 1300°С представлена на рисунке 1.
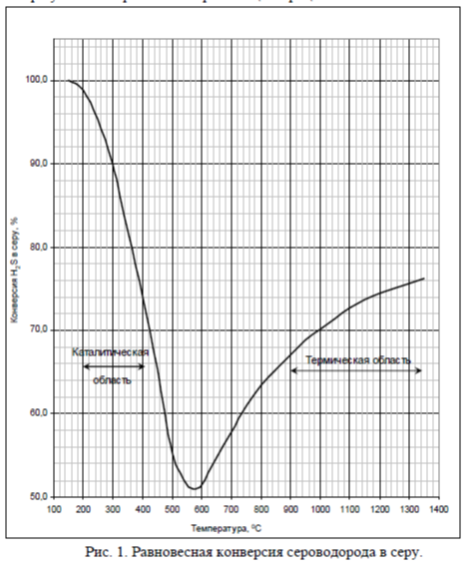
Рисунок 1. – Температурная зависимость термодинамически равновесной степени превращения H2S в парообразную элементарную серу
В процессе Клауса реакции протекают в трех зонах: 1 – высокотемпературная (выше 800°С), где превращение H2S в серу достигает 70 – 80% и возрастает с повышением температуры, так как сероводород начинает разлагаться на элементы; 2 – переходная зона, в которой снижение выхода серы при температуре 530 – 730°С обусловливается ассоциацией серы вида S2 в более высокомолекулярные виды S4, S6, S8; 3 – низкотемпературная каталитическая зона, в которой снижение температуры повышает степень конверсии.
Реакции в пламени ведут к превращению сероводорода в элементарную серу, образованию диоксида серы и разрушению примесей, которые могли бы дезактивировать катализатор. В высокотемпературной зоне пламени образуется сера в виде S1-2 в низкотемпературной – S3-8 [5 – 7].
Присутствие в кислом газе так называемые нежелательные компоненты (СО2, пары воды и углеводороды) могут вступать в побочные реакции, приводящие к снижению конверсии сероводорода в серу и образованию соединений, которые могут вступать в реакции образования серы на последующих (каталитических) стадиях процесса [8]:
Углеводороды сгорают с образованием СО2, СО, Н2О, Н2. При высоких температурах в пламени в результате взаимодействия углеводорода с парами серы образуется сероуглерод:
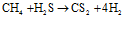 ,
,
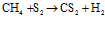 ,
,
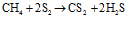 .
.
Свободный водород, образовавшийся при термической диссоциации сероводорода, восстанавливает диоксид углерода до оксида, который, взаимодействуя с серой, образует серооксид углерода:
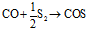 ;
;
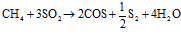 ;
;
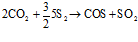 .
.
При понижении температуры газа реакция ведет в обратном направлении с образованием сероводорода, однако скорость обратной реакции с понижением температуры замедляется. Для полной конверсии сероокиси углерода необходимо проводить ее на катализаторе при температуре не ниже 350°С. Бокситовый катализатор, который применяется для контактного окисления сероводорода, может быть эффективен и для конверсии сероокиси углерода, однако наибольшая конверсия будет в случае применения активной Al2O3:
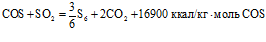 ;
;
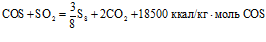 .
.
В связи с этим наиболее распространена схема с двумя каталитическими ступенями. При конвертировании газов, содержащих сероокись углерода, температура, до которой следует нагревать газы, поступающие в конвертор 1 ступени, принимается 230 – 280°С с тем, чтобы температура газов на выходе из 1-го конвертора была не менее 350°С для достижения полноты реакций взаимодействия COS и SO2.
Изучение механизма образования сероуглерода и серооксида углерода показало, что они образуются автономно. Образованию сероуглерода способствуют, в основном, ароматические углеводороды.
Вследсвие высокого содержания водяных паров в газе, полученном на термической стадии и поступающем в каталитический конвертор, CS2 и COS в присутствии катализаторов процесса частично гидролизуются. Скорость гидролиза возрастает с повышением температуры в конверторе (так, скорость гидролиза CS2 возрастает примерно вдвое на каждые 20°С). Температуру на выходе из первого конвертора поддерживают в пределах 320 – 360°С, при этом степень превращения COS достигает 90%, CS2 – 70 – 75% (несмотря на это, потери серы в виде CS2 и COS очень ощутимы).
Присутствие аммиака в поступающем на установку кислом газе, в случае если он целиком или частично проходит через печь не сгорая, также приводит к возникновению вторичных реакций образованию (за счет реакции с серой) отложений твердых аммонийных комплексов на самых холодных участках установки, возможному образованию оксида азота в присутствии кислорода, способствующего окислению диоксида серы в триоксид. Последний при взаимодействии с водой образует серную кислоту, которая наряду с коррозионными проблемами усиливает сульфатирование катализатора – оксида алюминия. В целях предотвращения этих реакций, необходимо удалять аммиак из сырьевого потока на стадии термического сжигания [5, 6].
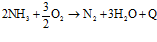 ;
;
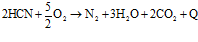 ;
;
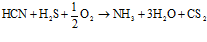 ;
;
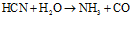 .
.
Сера обладает меньшей летучестью, чем другие компоненты газовой смеси, поэтому из технологического потока ее выводят конденсацией после реакционной печи и каждого каталитического конвертора. Это позволяет сдвигать равновесие реакции в сторону образования серы и уменьшать точку росы серы в газах, что, в свою очередь, дает возможность снизить температуру в каталитических конверторах, избегая осаждения серы на катализатор. Этот принцип лежит в основе работы каталитических стадий установок Клауса.
На основании термодинамических расчетов некоторые исследователи рекомендуют использование трех или четырех каталитических конверторов, работающих в стационарных условиях при весьма низкой температуре. В этом случае возможно достижение суммарного выхода серы, превышающего. Однако при современной технологии эти результаты не достигаются вследствие кинетических ограничений, например из-за отложения серы в порах катализатора [10].
Библиографический список
-
Абросимов А.А. Экология переработки углеводородных систем. М.: Химия, 2002, 608 с.
-
Банов П.Г. Процессы переработки нефти. М.: ЦНИИТЭнефтехим, 2003, Ч3, 504 с.
-
Чуракаев А.М. Переработка нефтяных газов. М.: Недра, 1983, 279 с.
-
Николаев В.Ю., Ляхов В.Д. Современная техника и технология производства газовой серы // Переработка газа и газового конденсата: науч.-технич. обз., М.: ВНИИЭгазпром, 1975, 60 с.
-
Широкова Г.С. Современные тендеции в развитии процесса Клауса. Пути решения задач по оптимизации работы установок производства серы // Материалы докладов международной конференции «Топливо и экология – 2009», М., 2009, С: 7 – 14.
-
Немировский М.С., Вихман А.Г., Мириманян А.А. Установка Клауса и выбросы диоксида азота // Нефтепереработка и нефтехимия, 2007, №12, С: 13 – 15.
-
Балыбердина И.Т. Физические методы переработки и использования газа. М.: Недра, 1988, 248 с.
-
Николаев В.В., Бусыгина Н.В., Бусыгин И.Г. Основные процессы физической и физико-химической переработки газа. М.: Недра, 1998, 184 с.
-
Щурин Р.М., Онопко Т.В., Калинина Н.В., Плинер В.М. Производство газовой серы методом Клауса // Промышленная и санитарная очистка газов обз. информация, М.: ЦИНТИХИМНефтемаш, 1986, 37 с.
-
Широкова Г.С. Переработка сероводородных газов в элементарную серу // Материалы докладов международной конференции «Топливо и экология – 2008», М., 2008, С: 48 – 51.
