Есть два широко известных способа получения энергии, использующих смешивание пресной и соленой воды.
Первый из них – механический способ. При этом способе генерации энергии сосуды с соленой и пресной водой разделены полупроницаемой мембраной. Благодаря осмотическому давлению уровень жидкости в сосуде с соленой водой поднимается, и этот перепад уровней жидкости можно использовать для генерации механической или электрической энергии. Недостатком этого способа является высокие потери энергии, поскольку электрическая мощность генерирует в два этапа.
Второй метод использует ионоселективные мембраны. Сосуды с пресной и соленой водой разделены с одной стороны катионселективными мембранами, с другой стороны- анион селективными. Ионы диффундируют от соленой воды к пресной, в результате чего на мембранах появляется разность потенциалов. В этом случае электрическая мощность генерирует в один этап. Недостатком приведенного способа является высокое электрическое сопротивление ионоселективных мембран.
Мы разрабатываем третий способ преобразования энтропии перемешивания пресной и соленой вод в электрическую энергию. В этом нам поможет хорошо знакомый концентрационный гальванический элемент.
Разумеется, раствор хлорида натрия не лучший рабочий раствор для концентрационного гальванического элемента. Мы можем использовать хлорсеребряные электроды (их потенциал зависит от концентрации ионов хлора), но они слишком дороги для широкомасштабного использования.
Наша идея- заменить электролит на более удобный.
Таким образом, схема нашего элемента:
соленая вода | | полупроницаемая мембрана | | рабочий раствор с высокой концентрацией | | пористая диафрагма | | рабочий раствор низкой концентрации | | полупроницаемая мембрана | | пресная вода.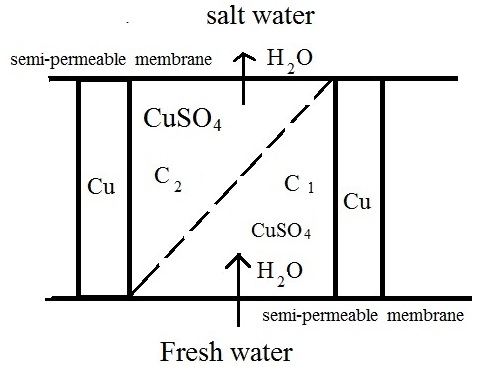
Рис.1. Схема ячейки гальванического элемента
На рисунке: С2> С1.
Осмотическое давление в рабочем растворе с низкой концентрацией выше, чем осмотическое давление в пресной воде, так что вода проходит через полупроницаемую мембрану в концентрации гальванического элемента и поддерживает низкую концентрацию электролита вблизи первого электрода.
Осмотическое давление соленой воды, наоборот, выше, чем осмотическое давление рабочего раствора высокой концентрации. Таким образом, вода проходит через полупроницаемую мембрану из концентрационного гальванического элемента и поддерживает высокую концентрацию электролита вблизи второго электрода.
Таким образом, раствор хлорида натрия не участвует в реакции, но поглощает воду из рабочего раствора высокой концентрации.
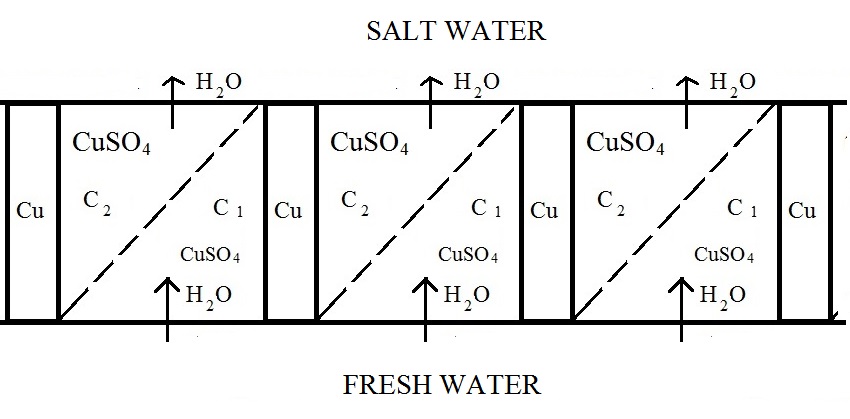
Элементы, приведенные на рисунке 1, могут быть соединены в каскад:
Рис.2. Каскад (последовательное соединение) гальванических элементов.
Также интересные результаты могут быть получены с использованием раствора серной кислоты в качестве рабочего раствора и электродов состава Pb/PbSO4.
В отличие от традиционных концентрации гальванических элементов, где разность потенциалов зависит логарифмически зависит от отношения концентраций растворов, в растворе серной кислоты мы имеем практическое линейную зависимость потенциала электрода от концентрации серной кислоты [1]. Этот эффект наблюдается из-за того, что гальванический элемент использует не только энтропии фактор, но и энергию экзотермической реакции растворения серной кислоты в воде.
Библиографический список
- Вассель С.С., Вассель Н.П. ИСПОЛЬЗОВАНИЕ НИЗКОПОТЕНЦИАЛЬНОЙ ТЕПЛОТЫ В ЭЛЕКТРОХИМИЧЕСКОМ ПРЕОБРАЗОВАТЕЛЕ. Современные научные исследования и инновации. 2014. № 4 (36). С. 21.
References
- Вассель С.С., Вассель Н.П. ИСПОЛЬЗОВАНИЕ НИЗКОПОТЕНЦИАЛЬНОЙ ТЕПЛОТЫ В ЭЛЕКТРОХИМИЧЕСКОМ ПРЕОБРАЗОВАТЕЛЕ. Современные научные исследования и инновации. 2014. № 4 (36). С. 21.

 Просмотреть статью на английском языке
Просмотреть статью на английском языке