Синтез модифицированных золей кремнезема – одно из перспективных мировых направлений, позволяющее значительно расширить области применения коллоидного кремнезема. Однако зачастую он связан с применением дорогостоящих реактивов и сложных химических процессов. Поэтому поиск нетрадиционных материалов и способов получения коллоидного кремнезема является актуальной задачей.
Ранее нами запатентован способ получения синтетического дигидрата сульфата кальция из техногенного сырья – высокоосновного сталеплавильного шлака, минералогический состав которого представлен островными ортосиликатами кальция-магния с изолированными кремнекислородными тетраэдрами [1]. Данный способ предусматривал обработку водной суспензии шлака концентрированной серной кислотой. Этот процесс необратим и, не доходя до состояния равновесия, из пересыщенного по отношению к сульфатам раствора, начинается их выделение в виде устойчивых в этих условиях соответствующих форм. Продуктом заявленного способа является поликомпонентный материал, содержащий до 80% дигидрата сульфата кальция и около 15% аморфного диоксида кремния.
Комплексная же переработка шлака подразумевает получение нескольких целевых продуктов: ультрадисперсного дигидрата сульфата кальция (CaSO4∙2H2О); наноразмерных кристаллов гетита (ά- FeOOH), а также железооксидных магнитных порошков и различных пигментов; коллоидной кремниевой кислоты и нанокомпозитов на ее основе. В связи с этим целесообразнее использовать соляную кислоту. Суть действия соляной кислоты заключается в реакции с составляющими шлака, в результате которой образуются легкорастворимые соли, переходящие в так называемый техногенный раствор. Солянокислая обработка шлака сопровождается, помимо образования солей металлов, выделением мономерной кремниевой кислоты.
Разработка коллоидно-химических принципов создания наноструктурированных систем и нанокомпозитов на основе коллоидной кремнекислоты предусматривает исследование особенностей золь-гель перехода в техногенных растворах кремниевой кислоты в присутствии катионов кальция, магния, железа и алюминия, и структурообразования сложных технических дисперсий в условиях постоянно изменяющегося состава и ионной силы дисперсионной среды и дисперсной фазы.
Для эксперимента использовалась водная суспензия шлака с Ж/Т=1:20 и массовой долей твердого компонента 4,76%. В суспензию вводилась концентрированная соляная кислота в стехиометрическом соотношении, рассчитанном на полное разложение минералов шлака. Выбор указанного состава обусловлен стабильностью образующихся золей в течение сравнительно длительного промежутка времени, что позволяет осуществить определение концентрации кремниевой кислоты во всем интервале рН.
Суммарную концентрацию «активных» кремниевых кислот, поликремниевых кислот в исследуемой дисперсии, а также общее содержание кремнекислоты определяли фотометрически по интенсивности окраски раствора с гептамолибдатом аммония. Этот метод является одним из наиболее доступных для изучения поликонденсации в растворах кремниевых кислот. Понятие «активная кремниевая кислота» включает мономер, димеры и низкомолекулярные поликремниевые кислоты.
Согласно полученным экспериментальным данным (рис. 1), максимальная концентрация «активных» фракций кремнекислоты в технической дисперсии зафиксирована при рН=2 (7,3 г/л), что обусловлено постепенным выщелачиванием минералов шлака. До рН≥5 концентрация мономерной кремниевой кислоты уменьшается незначительно (от 7 до 6 г/л). Резкое уменьшение концентрации мономерной кремниевой кислоты и соответственно увеличение концентрации поликремниевых кислот в сложных технических дисперсиях наблюдается при рН˃6. Именно это значение рН можно считать началом формирования геля кремниевой кислоты. Общее содержание кремниевых кислот, включающее и высокомолекулярные кислоты, составило 10 г/л, что соответствует 20% содержанию кремнезема в исходном шлаке.
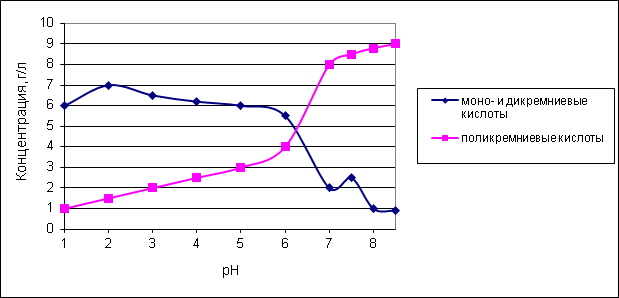
Рис. 1. Зависимость концентрации кремниевых кислот от рН
Одним из наиболее важных реологических параметров, характеризующих переход золя в гель, является вязкость, рост которой предшествует образованию геля. Установлено, что техническая дисперсия, полученная при обработке суспензии шлака соляной кислотой, обладает непродолжительным индукционным периодом, резкое увеличение вязкости зафиксировано уже при рН≥5 (рис. 2).
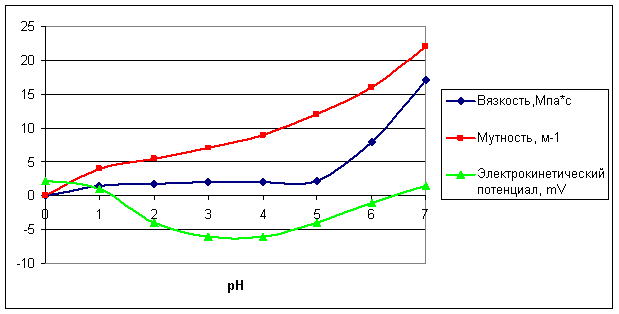
Рис. 2. Изменение вязкости, мутности и электрокинетического потенциала технической дисперсии
Гелеобразование может являться следствием протекания как реакций поликонденсации, так и коагуляции. Однако при коагуляции мутность золей растет в результате увеличения объема агрегированных частиц. Полученные нами результаты свидетельствуют о постепенном увеличении мутности дисперсии. Однако для окончательного подтверждения наличия коагуляционных процессов исследована зависимость дзета-потенциала на поверхности частиц коллоидной кремниевой кислоты от рН технической дисперсии. Установлено, что поверхность частиц коллоидной кремнекислоты вплоть до изоэлектрической точки заряжена положительно, что обусловлено сорбцией катионов Н+. Схему образования двойного электрического слоя при рН<2 можно представить следующим образом:[mH4SiO4nH+(n-x)Cl-]x+xCl-.
При увеличении рН>рНиэт=2,2 (вплоть до рН=4), частицы кремнекислоты кремниевой кислоты вступают в реакции поликонденсации. Схему образования ДЭС можно представить следующим образом: [mH4SiO4nH3SiO4-(n-x)H+]х-xH+.
Уменьшение отрицательного заряда на поверхности частиц кремнекислоты в техногенном растворе при рН>5 является следствием протекания коагуляционных процессов золя кремниевой кислоты под действием избытка ионов Са2+, способствующих нейтрализации потенциалопределяющих гидросиликат-ионов.
Известно, что коагуляция золей может протекать по концентрационному или нейтрализационному механизму. Концентрационная коагуляция происходит при добавлении к золю индифферентного электролита вследствие сжатия диффузного слоя противоионов и уменьшения абсолютного значения ζ -потенциала. Нейтрализационная коагуляция
происходит при добавлении к золю неиндифферентного электролита. При этом потенциалопределяющие ионы связываются в малорастворимое соединение, что приводит к уменьшению абсолютных величин термодинамического потенциала, а следовательно, и ζ -потенциала вплоть до нуля. Сделать вывод о механизме коагуляции в исследуемой дисперсии на основании результатов измерения электрокинетического потенциала не представляется возможным, так как при рН=8,5 визуализируется гель и дальнейшие измерения технически не осуществимы. Однако известно также, что частицы кремниевой кислоты коагулируют по концентрационному механизму, когда их размер превышает 100 нм, а нейтрализационная коагуляция свойственна частицам меньшего размера. В связи с этим, на следующем этапе работы определены размеры частиц коллоидной кремниевой кислоты в исследуемой дисперсии с помощью математической обработки спектров мутности.
Установлено, что радиус частиц кремниевой кислоты в технической дисперсии до рН=5 практически постоянен (≈20 нм). Увеличение размера частиц кремнекислоты при рН˃5 также подтверждает протекание процесса коагуляции, что согласуется с ранее полученными результатами. Максимального размера (80 нм) частицы кремнекислоты достигают спустя 1 час. Полученные результаты позволяют говорить о протекании нейтрализационной коагуляции в исследуемой дисперсии. Однако для окончательного подтверждения сделанного вывода нами проанализирован состав геля, подвергнутого старению, с помощью рентгенофазового анализа.
На полученной дифрактограмме (рис. 3) в области углов от 4 до 34° фиксируется неоднородное по высоте гало рентгеноаморфной фазы, что может указывать на наличие в системе двух различных по составу гелей.
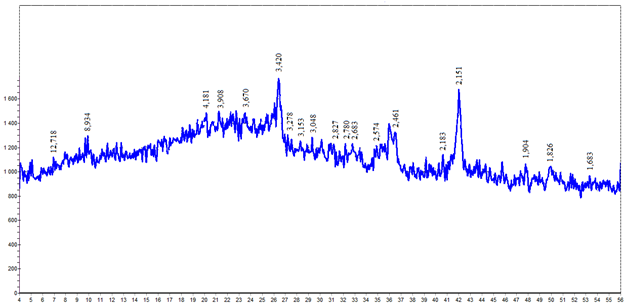
Рис. 3. Дифрактограмма полученного геля
С помощью картотеки ICPDF и электронной международной кристаллографической базы данных идентифицированы следующие соединения: НAlSi2O6 по аналитическим линиям при d/n = 3,420; 3,670; 3,153; 3,278; 1,904 Å, и 2Al2O3·2SiO2·H2O по величинам межплоскостных расстояний 8,934; 3,420; 2,461 Å. Слабые отражения при d/n = 12,718; 3,048; 2,827; 1,826; 1,683 Å принадлежат низкоосновному гидросиликату кальция типа пломбьерита (CaO·SiO2·2H2O). Таким образом, полученный гель имеет силикатную природу, в которой выделяются две составляющие: кальциевая и алюминатная.
Для подтверждения полученных результатов проведены дифференциально-термический анализ и рентгенофазовый анализ термообработанного при 1000°C геля. Установлено, что продуктами термообработки являются кварц, силиманит (Al2O3·SiO2) и волластонит (СаО·SiO2).
Таким образом, наличие в анализируемом образце гидросиликатов различного состава окончательно подтверждает протекание в исследуемой дисперсии нейтрализационной коагуляции.
Гидролизом гидросиликатов кальция может быть обусловлена слабощелочная реакция технической дисперсии. Схематично уравнение гидролиза гидросиликата кальция можно представить следующим образом:
SiO44- + H2O ↔ HSiO43- + OH-
Значение растворимости гидросиликата кальция (2·10-4 моль/л) и константы гидролиза кремниевой кислоты по второй ступени (2·10-12) позволили рассчитать ожидаемый уровень рН – 11,2. Таким образом, параллельно протекающие процессы гидролиза хлоридов железа, приводящие к понижению рН, и силикатов кальция, сопровождающиеся увеличением рН, дают усредненное значение рН = 7,5 – 8,0.
Следует отметить, что максимальная концентрация катионов Са2+, Fe3+, Аl3+ в технической дисперсии зафиксирована при рН=4, что обусловлено постепенным разложением минералов шлака. С ростом рН наблюдается уменьшение концентрации указанных катионов. Однако при рН≈6,8 зафиксировано увеличение концентрации катионов Са2+. Этот факт также подтверждает образование и гидролиз гидросиликатов кальция.
В общем виде схему протекающих в технической дисперсии процессов можно представить следующим образом:
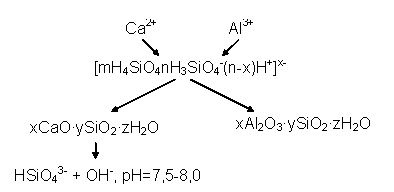
Однако следует отметить, что применительно к реальной многокомпонентной дисперсной системе, содержащей помимо коллоидной кремниевой кислоты хлориды металлов, а также в условиях постоянно изменяющегося рН среды, механизм более сложный.
Так, например, гидролиз хлорида алюминия может сопровождаться образованием золей гидроксида алюминия, которые, в зависимости от рН исследуемой дисперсии, заряжены отрицательно или положительно. В условиях существования двух разноименно заряженных золей возникает явление соосаждения коллоидных растворов с кристаллизацией в дальнейшем аллофаноподобных гидросиликатов алюминия.
Проведенные экспериментальные исследования позволили сформулировать основные требования к технологическим параметрам переработки шлака и выделения коллоидной кремниевой кислоты, а также предложить схему указанного процесса (рис. 4).
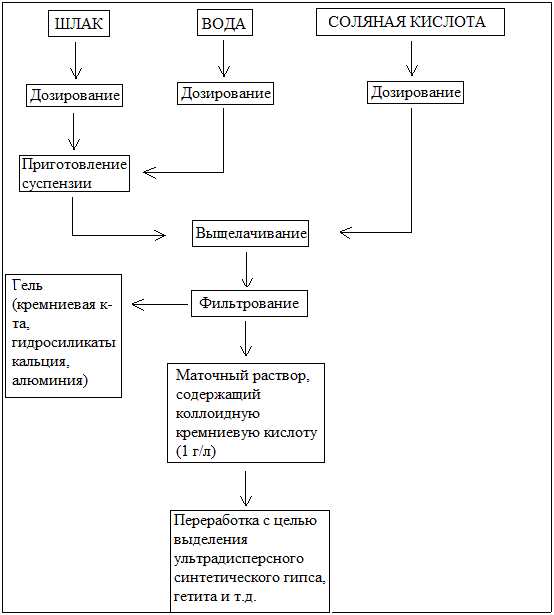
Рис. 4. Технологическая схема переработки шлака
В технологической схеме предусмотрено приготовление водной суспензии шлака с массовой долей твердого компонента 4,76%, выщелачивание минералов шлака концентрированной соляной кислотой (по ГОСТ 3118-67) в стехиометрическом соотношении. В силу того, что коагуляционные процессы в технической дисперсии сопровождаются интенсивным гелеобразованием еще до достижения нейтральной реакции среды, процесс выщелачивания шлака целесообразнее осуществлять при кипячении. В этом случае гелеобразные продукты выпадают в осадок, который отделяется декантацией или фильтрованием. Остаточное содержание кремниевых кислот в маточном растворе не превышает 1 г/л.
Полученный нанокомпозиционный материал на основе кремниевой кислоты, содержащий низкоосновные гидросиликаты кальция, целесообразно рекомендовать для использования в качестве наноинициатора твердения вяжущих различного состава.
Проведенные экспериментальные исследования особенностей золь-гель перехода в техногенных растворах кремниевой кислоты позволят в будущем не только управлять ходом процесса, но и, в зависимости от назначения, получать продукт с заранее заданными свойствами. Это, в свою очередь, является необходимым условием разработки научно–обоснованных критериев комплексной переработки высокоосновных сталеплавильных шлаков, а также наиболее полного извлечения продукта и минимизации затрат.
Библиографический список
- Способ получения дигидрата сульфата кальция: пат. 2371408 Рос. Федерация / В.А. Белецкая, Е.Л. Проскурина, И.В. Каблучко; заявитель и патентообладатель Белгородский государственный университет. - № 2008114231; заявл. 2008.04.11; опубл. 2009.10.27.
- Румянцева, Е. Л. Золь-гель процессы при разложении высокоосновного шлака кислотой [Текст] / Е. Л. Румянцева // Молодой ученый. — 2013. — №7. — С. 27-30.
