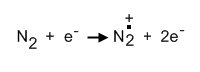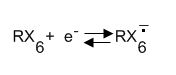Электроны низких энергий [1] могут образовываться при ионизации газа (например, азота) электронами высоких энергий:
Органические молекулы со значительным сродством к электрону (энергия акцептирования электрона частицей при абсолютном нуле) способны захватывать такие электроны с образованием анион-радикалов (частица имеет отрицательный заряд и неспаренный электрон) [2]:
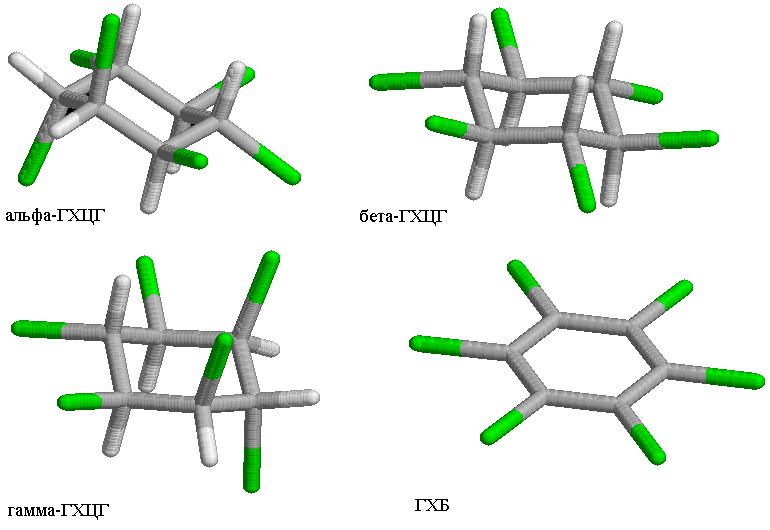
Были рассчитаны значения энергии акцептирования электрона для некоторых пестицидов полуэмпирическими методами (АМ1, PM3, MINDO3, MNDO) [2]. Структуры молекул данных пестицидов представлены на рис. 1.
Рис. 1. Молекулы пестицидов. Метод – АМ1.
Энергетическая диаграмма показана на рис. 2. Наибольшая энергия акцептирования электрона молекулой характерна для ГХБ.
Рис. 2. Энергетическая диаграмма. Метод – АМ1. Разность между энергиями молекулы и анион-радикала соответствует энергии акцептирования электрона.
В экспериментах молекулы захватывают электроны при различных температурах. Отметим, что повышение температуры от 0 до 573 Kсоответствует уменьшению сродства на 0.12 эВ/моль [3]. Присоединение электрона молекулой сопровождается изменением ядерных (атомных) координат. Например, на увеличение расстояния между атомами необходимо затратить энергию. Оценка энергии изменения ядерных координат сопоставлением потенциала ионизации анион-радикала и сродства к электрону молекулы дает следующие значения: ГХБ – 0.79, альфа-ГХЦГ – 1.94, бета-ГХЦГ – 2.10, гамма-ГХЦГ – 1.92 (эВ/моль). Это большие величины. Меньшее значение для ГХБ объясняется наличием сопряженной системы. Рассмотрена простейшая термодинамическая модель. Частица, присоединившая электрон может какое-то время находится в возбужденном состоянии, а затем передать часть энергии другой частице в результате соударения:
В более сложных моделях учитывается возможность диссоциативного захвата электрона [4]. Образовавшийся при диссоциативном захвате электрона радикал обладает значительным сродством к электрону и, с термодинамической точки зрения, следует ожидать акцептирования электрона указанной частицей. При этом образуется анион (рис. 3). Если для изучения подобного рода процессов использовать детектор электронного захвата, в котором регистрируется уменьшение тока электронов к аноду при их захвате различными частицами, то теоретически можно допустить случай уменьшения тока в результате захвата электронов молекулами, затем возрастание тока и вновь его уменьшение из-за присоединения электронов радикалами.
Рис. 3. Энергетическая диаграмма для бета-ГХЦГ. Метод –АМ1.
Отметим, что возможна рекомбинация (соединение) анион-радикалов друг с другом с образованием дианионов и рекомбинация радикалов с образованием молекул (хотя имеются стерические препятствия).
Известно, что при температуре около 500 К анион-радикал ГХБ не диссоциирует [4].
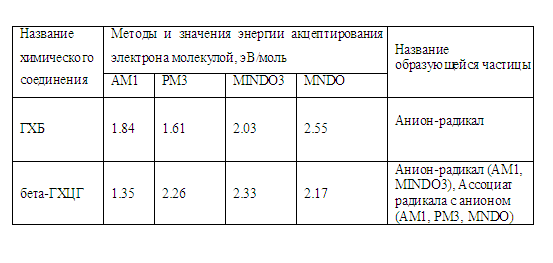
В таблице 1 представлены данные для сравнения результатов, полученных разными полуэмпирическими методами.
Таблица 1
Результаты моделирования свидетельствуют о том, что в одних случаях акцептирование электрона молекулой приводит к образованию анион-радикала, а в других – ассоциата радикала с анионом. Радикал, образовавшийся при распаде ассоциата, способен акцептировать электрон с освобождением значительного количества энергии. Данные компьютерного эксперимента не противоречат хроматографическим данным с использованием детектора электронного захвата (имеется в виду неодинаковый механизм взаимодействия электронов с различными молекулами) [5].
Библиографический список
- Ray SG, Daube SS, NaamanR. On the capturing of low-energy electrons by DNA. J. Proc. Natl Acad. Sci. USA 2005;102:15-19.
- Тодрес З.В. Ион-радикалы в органическом синтезе. М.: Химия. 1986. 237 с.
- J. C. Rienstra-Kiracofe, G.S. Tschumper, H.F. Schaefer III. Atomic and Molecular Electron Affinities: Photoelectron Experiments and Theoretical Computations//Chem. Rev. 2002. 102. P. 231 – 232.
- E.C.M. Chen, E.S. Chen. The Calculation of Electron Affinities and Bond Dissociation Energies of Pesticides and Explosives Analyzed in Negative Ion Mobility Spectrometry//IJIMS. 2002. P. 11 – 14.
- Гиошон Ж., Гийемен К. Количественная газовая хроматография для лабораторных анализов и промышленного контроля: В 2-х частях. Ч. I: Пер. сангл.-М.:Мир, 1991. С. 535.