Введение
Олигонуклеотид – это короткий фрагмент нуклеиновой кислоты менее 50 нуклеотидов в длину. В течение последних 20 лет, смысл расширился, чтобы включать в себя все химически синтезированные нуклеиновые кислоты, независимо от длины. Первая публикация о направленном химическом синтезе олигонуклеотида появилась в 1955 году.
С тех пор, миллионы олигонуклеотидов синтезируются каждый год для использования в лабораториях по всему миру. Для большинства исследований нужны лишь небольшие количества ДНК. Гораздо большее количество ДНК (10 мкмоль или более) необходимы для использования в биофизических исследованиях (ЯМР и рентгеновской кристаллографии) поэтому, чтобы обеспечить синтез столь больших количеств, были разработаны методы твердофазного синтеза, что позволяет использовать олигонуклеотиды в качестве молекул лекарственного средства (например, антисмысловые олигонуклеотиды).
Синтез ДНК или РНК олигонуклеотидов относится к химическому синтезу фрагментов нуклеиновых кислот с определенными химическими структурами или последовательностей в различных размерах.
Принцип твердофазного синтеза впервые был разработан и применен для синтеза полипептидов Роберта Брюса Меррифилда, американского биохимика, который получил Нобелевскую премию по химии в 1984 году за изобретение твердой фазы синтеза пептидов. Он понял, что ключ к успешному синтезу заключается в закреплении первого мономера к нерастворимой полимерной твердой фазе. Другие мономеры затем могут быть соединены, один за другим, к неподвижному терминальному концу растущего полимера. В конце синтеза, завершенная полимерная цепь может быть отсоединена от нерастворимого полимера и очищена. Этот процесс был оптимизирован на протяжении многих лет, чтобы стать высокоэффективным и теперь стал принципиально важным методом, используемым в автоматизированных олигонуклеотидных синтезаторах.
Для обеспечения успешного синтеза олигонуклеотидов необходимы следующие условия:
- Все реагенты должны быть растворимы в неводных растворителях.
- Амино- и гидроксильные группы нуклеотидных оснований и углеводных остатков должны быть соответствующим образом блокированы.
- Защитные группы, введенные в процессе синтеза, должны быть стабильными в условиях удлинения цепи при образовании межнуклеотидной фосфодиэфирной связи.
- Защитные группы должны быть достаточно лабильными, чтобы их можно было удалить в конце синтеза, не повредив продуктов реакции.
Функции олигонуклеотидов и перспективы их применения
В настоящее время олигонуклеотиды и их аналоги широко используются в различных областях, таких как медицина и в молекулярно-биологических исследованиях, а также рассматриваются в качестве перспективных терапевтических средств и зондов для молекулярной диагностики.
За последние 20 лет относительно хорошо были изучены только два типа аналогов нуклеиновых кислот с формально электронейтральным остовом – пептидные нуклеиновые кислоты и фосфордиамидные морфолиноолигонуклеотиды. Аналоги обоих типов способны к комплементарному связыванию с природными молекулами ДНК и РНК, и в силу этого они нашли применение как в молекулярной биологии, так и, в особенности, в медицине в качестве потенциальных лекарственных препаратов.
Кроме того, с развитием ДНК-технологий появилась возможность изучения экспрессии известных генов, определения мутаций в геномах различных организмов и проведения диагностики ряда инфекционных заболеваний. В решении этих задач наиболее перспективным является использование ДНК-чипов, представляющих собой небольшие пластины с нанесенными на их поверхность фрагментами ДНК.
Способ создания ДНК-чипов объединяет методы, основанные на адресном синтезе олигонуклеотидов непосредственно на поверхности чипа. Синтез проводят путем поэтапного добавления к растущей олигонуклеотидной цепи нуклеотидов, содержащих на 5’-конце лабильную защитную группу, снятие которой возможно под действием светового излучения, электрического напряжения или в ходе кислотного гидролиза.
Показано, также, что ген-направленные олигонуклеотиды, в зависимости от выбранного гена-мишени, отличаются значительным разнообразием модулирующих эффектов на опухолевые ткани, начиная от замедления и остановки пролиферации опухолевых клеток и заканчивая подавлением их инвазивных свойств.
Противоопухолевые препараты на основе нуклеиновых кислот представляют собой высокоспецифичный инструмент модуляции экспрессии генов. Подавление ряда генов, аномально высокая экспрессия которых возникает при неопластической трансформации, можно осуществить с помощью препаратов на основе нуклеиновых кислот, таких как антисмысловые олигонуклеотиды (asON). В общем, механизм подавления экспрессии генов заключается в их комплементарном связывании с мРНК-мишенью, после чего целевая мРНК либо подвергается расщеплению, либо блокируется процесс ее трансляции.
asON представляют собой синтетические одноцепочные ДНК длиной 15-20 нуклеотидов. В последнее время были получены asON, способные препятствовать транспорту сплайсированной мРНК из ядра в цитоплазму, а также asON, которые в результате блокирования сайта сплайсинга в пре-мРНК способны приводить к экспрессии альтернативного варианта белка.
Ввиду того, что природные олигодезоксирибонуклеотиды в культуре клеток и в условиях in vivo подвергаются быстрой деградации под действием нуклеаз, для повышения их стабильности в структуру asON вводят различные химические модификации.
Химический синтез олигонуклеотидов
Твердофазный синтез широко используется в синтезе пептидов, синтезе олигонуклеотидов, синтезе олигосахаридов и комбинаторной химии. Твердофазный химический синтез был изобретен в 1960-е годы Брюсом Меррифилдом, и был удостоен Нобелевской премии по химии в 1984 году.
Твердофазный синтез осуществляют на твердом носителе, между фильтрами, в столбцах, которые пропускают все реагенты и растворители. Твердофазный синтез имеет ряд преимуществ по сравнению с синтезом в растворе:
обеспечивает высокую скорость реакции
примеси и избыток реагентов смываются, поэтому очистка после каждого шага не требуется
процесс поддается автоматизации на твердофазных синтезаторах с компьютерным управлением.
Твердые носители (называемые также смолами) представляют из себя нерастворимые в воде частицы, как правило, 50-200 мкм в диаметре, к которым олигонуклеотид присоединяется в процессе синтеза.
Имеются данные, что одним из наиболее эффективных материалов, которые можно использовать в качестве твердого носителя, является пористое стекло. Оно достаточно жесткое и не способно к набуханю. В его глубоких порах, происходит синтез олигонуклеотидов. Стекло содержит 500 Å (50 нм) поры, которые подходят для синтеза коротких олигонуклеотидов. Тем не менее, оно плохо подходит для синтеза олигонуклеотидов более 40 оснований в длину. Это связано с тем, что растущий олигонуклеотид блокирует поры и уменьшает диффузию реагентов через матрицу.
Твердые носители для обычного синтеза олигонуклеотидов, как правило, изготовлены с нагрузкой 20-30 мкмоль нуклеозида на грамм смолы. Синтез олигонуклеотидов при более высоких нагрузках становится менее эффективным вследствие стерических затруднений между соседними цепями ДНК, присоединенных к смоле.
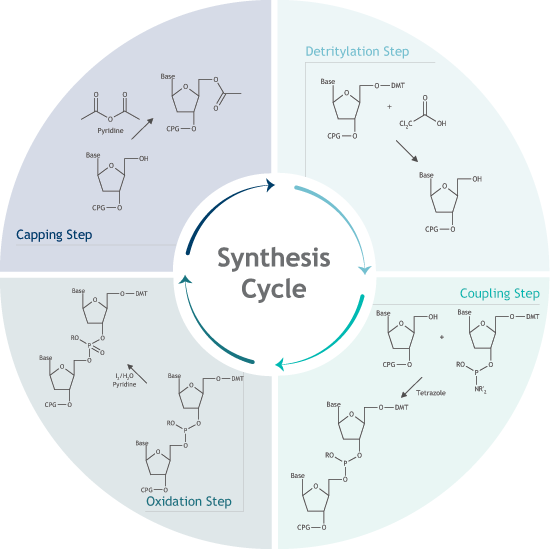
Этапы химического синтеза олигонуклеотидов
Фосфорамидатный олиго-синтез протекает в 3′- к 5′-направлении (противоположном 5′- к 3′-направлении биосинтеза ДНК в репликации ДНК). Один нуклеотид добавляется за синтез цикла.
В начале олигонуклеотидного синтеза первый нуклеозид предварительно присоединяют к смоле (носителю), и выбираются колонны синтеза A, G, C или T в зависимости от нуклеозида на 3′-конце желаемого олигонуклеотида. Закрепленный нуклеозид имеет 5′-ДMT защитную группу (ДМТ = 4,4′-диметокситритил), роль которой состоит в предотвращении полимеризации, и эта защитная группа должна быть удалена (детритилирование). Механизм детрилирования показан на рисунке 3.
После детритилирования, закрепленный нуклеозид готов реагировать со следующим основанием, который добавляется в виде нуклеозид-фосфорамидатного мономера. Большой избыток соответствующего нуклеозида, смешивают с активатором (тетразолом или его производными). Диизопропиламиногруппа нуклеозида протонируется активатором, и, таким образом, превращается в хорошо отсоединяющуюся группу. Она быстро вытесняется 5′-гидроксильной группой связанного нуклеозида, создавая фосфит триэфир (рис. 4).
Нуклеозидные фосфорамидиты достаточно стабильны в инертной атмосфере, и могут быть получены в больших количествах, доставляться по всему миру, и храниться в виде сухого твердого вещества в течение нескольких месяцев перед использованием.
Однако даже при высокоточных работах по синтезу олигонуклеотидов, остается вероятность, что там будет несколько непрореагировавших 5′-гидроксильных групп, которые будут доступны для участия в следующей стадии. Если подобное нарушение не остановить, они будут накапливаться с каждым последующим циклом, и конечный продукт будет сложной смесью олигонуклеотидов, большинство из которых будет нести неправильную генетическую информацию.
Поэтому метод ацетилирования 5′-гидроксильных групп делает их инертным по отношению к последующей реакции. Это необходимо также и для минимизации примесей.
Фосфит-триэфир (Р (III)), образованный на стадии присоединения неустойчив к кислотам и должен быть преобразован в стабильную форму (P (V)). Это достигается за счет окисления йода в присутствии воды и пиридина (рис. 5). Полученный фосфотриэфир фактически представляет собой ДНК ось, защищенную 2-цианоэтил группой. Группа цианоэтила предотвращает нежелательные реакции с фосфором во время последующих циклов синтеза.
После этого, ДМТ-защитная группа на 5′-конце цепи ДНК должна быть удалена так, чтобы первичная гидроксильная группа могла вступить в реакцию со следующим нуклеотид-фосфорамидатом. Реакция удаления защитной группы с помощью трихлоруксусной кислоты в дихлорметане протекает быстро. Цикл повторяется, один раз для каждой основы, до получения требуемого олигонуклеотида.
Далее необходимо отсоединить синтезированный олигонуклеотид от твердого носителя. В этом случае используется сукцинил. Разделение возможно при обработке концентрированным водным раствором аммиака при комнатной температуре в течение одного часа (рис. 6).
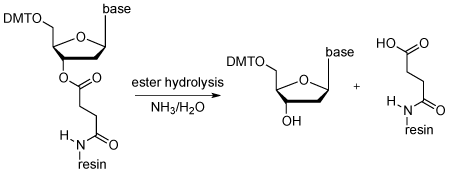
Рис.6. Механизм отделения олигонуклеотида от твердого носителя в концентрированном водном растворе аммиака.
Реакция расщепления осуществляется автоматически на некоторых синтезаторах, и аммиачный раствор, содержащий олигонуклеотид, поступает в стеклянный флакон. В качестве альтернативы, расщепление может быть осуществлено вручную путем принятия колонки от синтезатора и промыванием в шприцах, содержащих гидроксид аммония.
Олигонуклеотид растворяется в концентрированном водном растворе аммиака, а последующий нагрев позволяет удалить защитные группы из гетероциклических оснований и фосфатов. Водный раствор затем удаляют выпариванием и олигонуклеотид готов к очистке.
Кроме ДМТ-защитной группы, необходимы также дополнительные защитные группы и для аденина, цитозина и гуанина (рис.7). Однако для тимина в этом нет необходимости.
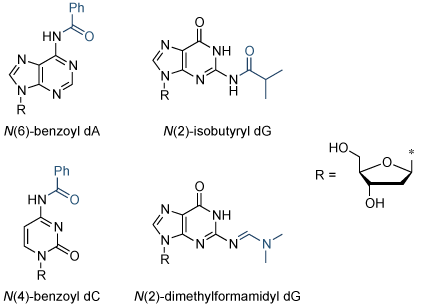
Рис.7. Структуры защитных групп, обычно используемые для защиты адениновых, цитозиновых и гуаниновых оснований во время фосфорамидатного синтеза ДНК олигонуклеотидов.
Выводы
1. Искусственно синтезированные олигонуклеотиды находят все более широкое применение в различных областях науки, а методы их получения все более совершенствуются, что позволяет синтезировать достаточное количество олигонуклеотидов для лабораторных экспериментов и для создания терапевтических препаратов.
2. На сегодняшний день, самым распространенным методом синтеза олигонуклеотидов остается метод твердофазного синтеза, который позволяет существенно ускорять процесс получения олигонуклеотидов, а также уменьшать объемы затраченных реактивов.
3. Твердофазный синтез включает в себя четыре основных этапа, в ходе которых возникает необходимость в защите фосфорных и аминогрупп для предотвращения возникновения спонтанных реакций.
Библиографический список
- Avery, O.T. Studies on the chemical nature of the substance inducing transformation of Pneumococcal types/ O.T. Avery, C.M. MacLeod and M. McCarty// J. Exp. Med. – 1944. – №79. – P.137-158.
- Bannwarth, W. Synthesis of Oligodeoxynucleotides by the Phosphite-Triester Method Using Dimer Units and Different Phosphorous-Protecting Groups/ W. Bannwarth// Helvetica Chimica Acta. – 1985. – V. 68, Issue 7. – P. 1907–1913.
- Dirin, M. Fragment-based solid-phase assembly of oligonucleotide conjugates with peptide and polyethylene glycol ligands / M. Dirin, E. Urban, C.R. Noe, J.Winkler// Eur J Med Chem. – 2016. – P.132-142
- Berner, S. Studies on the role of tetrazole in the activation of phosphoramidites/ S. Berner, K. Muhlegger, H. Seliger// Nucleic Acids Res. – 1989. – №17(3). – P.853-864
- Купрюшкин, М. С. Фосфорилгуанидины. Новый класс аналогов нуклеиновых кислот/ М.С. Купрюшкин, Д.В. Пышный, Д.А. Стеценко // Acta Naturae (русскоязычная версия). – 2014. – №4 (23). – С.123-125.
- Гарафутдинов, Р. Р. Химические аспекты создания ДНК-чипов/ Р.Р. Гарафутдинов, И.С. Шепелевич, А.В. Чемерис, Р.Ф. Талипов // Вестник Башкирск. ун-та. – 2005. – №1. – С.49-54.
- Патутина, О. А. Новейшие подходы к лечению онкологических заболеваний: противоопухолевые препараты на основе ген-направленных нуклеиновых кислот/ О.А. Патутина, Н.Л. Миронова, В.В. Власов, М.А. Зенкова// Acta Naturae (русскоязычная версия). – 2009. – №2 . – С.47-66.
- Rodriguez, A.A. Conversion of adenine to 5-amino-4-pyrimidinylimidazole caused by acetyl capping during solid phase oligonucleotide synthesis/ A.A. Rodriguez, I. Cedillo, A.K. McPherson// Bioorg Med Chem Lett. – 2016. – P. 30653-9.