Актуальность. На данный момент большое количество данных и результатов научных исследований позволяет выделить наследственные тромбофилии в отдельную группу причин невынашивания беременности. Например, в анамнезе пациенток с неоднократными безуспешно предпринятыми попытками искусственного оплодотворения данная патология как составной фактор причин таких результатов встречается с частотой до 90 % [1, №1, с. 49-59].
В норме гемостаз беременной женщины изменяется в сторону гиперкоагуляции. В частности происходит увеличение факторов VII, VIII, X и фактора Виллебранда, а так же заметное увеличение содержания фибриногена в крови. Увеличиваются маркеры образования тромбина, такие как F1 и F2 и тромбин-антитромбиновые комплексы (ТАТ) [2, URL]. В то же время происходит заметное снижение антикоагулянтной активности, включая снижение белка S. Активность фибринолитической системы так же снижена в связи с увеличением в 5 раз ингибитора активатора плазминогена 1 (PAI-1), а так же ингибитора активатора плазминогена-2 (PAI-2), в частности, во время третьего триместра беременности [3, URL]. Эти изменения системы гемостаза задуманы природой как «подушка безопасности» в парародовый (перипартум) период, но так же могут привести к осложнениям со стороны как матери, так и плода. Для матери этот риск начинается с момента зачатия и продолжается в послеродовом периоде, по последним данным риск распространяется по крайней мере на 12 недель [4, №370, с. 307-315]. Для плода во время беременности в состав рисков входят преэклампсия, отслойка плаценты, задержка роста плода, поздний или ранний выкидыш, внутриутробная смерть и мертворождение.
Так же к развитию тромбозов предрасполагает не только гиперкоагуляция крови, но и местные причины в виде стаза венозной крови в нижних конечностях в связи с механической обструкцией венозного оттока беременной маткой беременной маткой.
Риск развития осложнений, связанных с изменениями в системе гемостаза, гораздо выше у женщин, имеющих в анамнезе наследственную или приобретенную тромбофилию. Тестирование на тромбофилию наследственной формы в последнее время проводится всё чаще в связи с растущим количеством беременных и всё более успешным применение ВРТ, в связи с чем заметно увеличилась возрастная планка беременных женщин, а так же, соответственно, количество и качество медицинских осложнений [5,URL]. Существует гипотеза, что тромбофилии могут привести к развитию плацентарной недостаточности вследствие плацентарного тромбоза сосудов, ведь, как известно, кровообращение в плаценте зависит от равновесия антикоагулянтных и прокоагулянтных механизмов. Таким образом, при тромбофилии будет нарушено данное соотношение в сторону гиперкоагуляции и как следствие имплантация трофобласта становится неполноценной, что ведет к бесплодиям, привычному невынашиванию беременности, отслойке плаценты, HELLP-синдрому, а так же безрезультатным попыткам ЭКО.
Наследственные тромбофилии обусловлены генетическим полиморфизмом, который ведет к проявлению болезни не сам по себе, но с помощью провоцирующих факторов – например, беременность, хирургическое вмешательство, опухоли или травмы и т.д. Важными полиморфизмами, приводящими к наследственной тромбофилии являются фактор V Лейдена (FVL), протромбинового G20210A и MTHFR C677T и A1298C. Наиболее распространенной из названных выше является мутация фактора V Лейдена. Этот полиморфизм – результат замены аргинина на аминокислоту глютамин в положении 506 в факторе V, что ведёт к тромбозам в виду того, что в результате мутации снижается чувствительность фактора V к деактивации активированным белком C [6, URL].
Большинство исследований мировой литературы и отечественные данные подтверждают, что такой диагноз как тромбофилия является наиболее частой причиной течения беременности с различными осложнениями. Например, в 75% случаях осложненных беременностей регистрируется синдром потери плода, а 80% – преждевременная отслойка плаценты, и, наконец, практически в 100% тромбофилии имеют место в случаях венозной тромбоэмболии [7, URL]. Особое значение осложнений стоит рассмотреть при сочетании тромбофилий и столь популярном сейчас методе оплодотворения ЭКО. В большинстве случаев при ЭКО проблема невынашивания беременности проявляет себя в первом триместре. По сути программы ЭКО и ПЭ предполагают применение больших доз препаратов гормональной природы, в том числе гонадотропины, которые имеют влияние на выработку эндогенных яичниковых гормонов, что в результате может привести к отрицательным последствиям со стороны системы гемостаза. Как говорилось выше, при изменении системы гемостаза в сторону гиперкоагуляции может быть нарушен важнейший этап беременности – период имплантации трофобласта. Таким образом, сочетание физиологической гиперкоагуляции, тромбофилий (которые имеют далеко не последнее значение) и ЭКО, становится понятно, что один из самых уязвимых периодов – первый триместр беременности.
Современный уровень знаний, а также высокое качество медицинской помощи позволяют задолго до наступления беременности задуматься о профилактике репродуктивных потерь и начинать ее в предгравидарном периоде, что представляется наиболее эффективным.
Цель исследования. Проанализировать структуру генетически обусловленных тромбофилии в формировании ранних эмбриональных потерь после ВРТ у пациенток с бесплодием и привычным невынашиванием беременности на базе ГБУЗ ТО «Перинатальный центр» г. Тюмень.
Материалы и методы исследования. В ходе исследования был проведен ретроспективный анализ 131(100%) амбулаторных карт пациенток ГБУЗ ТО «Перинатального центра» (г. Тюмень) с диагнозами привычное невынашивание беременности (32 карты – 24,4%) и бесплодие (99 карт – 75,6%) (См. рис. 1).
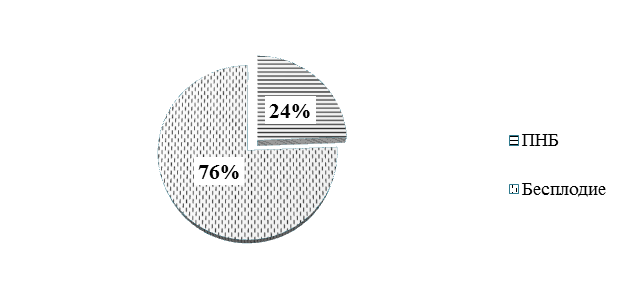
Рис. 1. Структура исследуемой группы.
Для исследования проводился забор периферической крови и ее анализ для определения генетических полиморфизмов, ассоциированных с риском развития тромбофилии, методом ПЦР в режиме реального времени при помощи комплекта реагентов «КардиоГенетика Тромбофилия», производитель «ООО ДНК-Технология» (Россия). Комплект реагентов предназначен для использования в лабораториях, оснащенных детектирующими амплификаторами для ПЦР с детекцией результатов в режиме реального времени.
В обследуемую группу вошли пациенты в возрасте от 20 до 45 лет.
Результаты исследования и их обсуждение. В группе с диагнозом привычное невынашивание беременности данные расположились следующим образом: наибольшее распространение данный диагноз имеет в группе 31-35 лет (13 пациенток – 40,6%), далее в группах 26-30 лет и 36-40 лет (по 8 пациенток – 25% соответственно), и наконец в группах старше 41 года (2 пациентки – 6,3%) и 1 в возрасте 20-25 лет (3,1%).
В группе с диагнозом бесплодие данные расположились немного иначе: 36-40 лет (35 пациенток – 35,4%), 31-35 лет (31 пациентка – 31,3%),
26-30 лет (22 пациентки – 22,2%), старше 41 лет (10пациенток -10,1%) и 20-25 лет – 1(1%). Средний возраст женщин с диагнозом бесплодие 35лет ± 1 год (См. рис. 2).
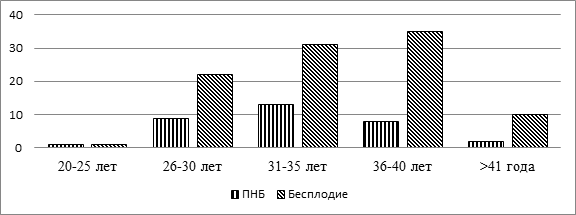
Рис. 2. Возрастная структура пациенток в диагнозами ПНБ и бесплодие.
Из группы по ПНБ 22 пациентки(69%) (при обращении) предъявляли жалобы на потери беременности в первом триместре, 6(19%) – на потери беременности во втором триместре, 2(6%) потеряли беременности на доношенном сроке (37 и 39 недель) и 1 – на гибель плода раннем неонатальном периоде (3%).
По медицинским показаниям в условиях гинекологического отделения во втором триместре были прерваны 3 беременности(9,4%) и 2(6,25%)пациентки от прерывания беременности отказались (из них у одной – в 3 триместре антенатальная гибель плода, вторая родоразрешилась доношенным ребенком в сроке 38-39 недель, который умер на первые сутки от врожденного порока сердца несовместимого с жизнью).
В ходе исследования так же выяснилось, что у 5(15,6%) пациенток диагностирован ВПР плода. Из них в 1 случае ВПР ССС плода, в 3 – встречались грубые дефекты развития невральной трубки (2 – анэнцефалия и 1 – незаращение позвоночника), ВПР ЖКТ в 1 случае.
Характер наследственных тромбофилических синдромов (n=131) распределился следующим образом:
В 87,2% случаев (96 пациенток) наблюдалась мутация в гене PAI-1(из них 35 – гомозиготы, 61 – гетерозиготы). По данным литературы именно эта аномалия приводит к частым отрицательным результатам ЭКО и ИКСИ. В данном случае эффективность лечения бесплодия при помощи ВРТ при наличии мутации в гене PAI-1 была положительной только у 38 пациенток (среди них 28 – мутация по гетерозиготной аллели, 10 – по гомозиготной), беременность которых завершилась родоразрешением. У 44 пациенток (40% случаев), наблюдалось невынашивание (из них у 24 мутация в гомозиготной аллели, а у 20 – в гетерозиготной).
В 60,9% случаев (67 пациенток) наблюдалась мутация в гене ITGA-2. Гомозиготная аллель обнаружена в 15 случаях, гетерозиготная аллель – 52 случая. Эффективность ВРТ была положительной у 48 пациенток (из них у 14 мутированный ген ITGA-2 находился в гетерозиготной аллели, а у 3– в гомозиготной). Проведение ЭКО и ИКСИ не дало результатов у 38 пациенток (из них 32 случая мутация в гетерозиготной аллели, а в 6 случаях – в гомозиготной аллели).
В 35,4% случаев (39 пациенток) наблюдалась мутация в гене ITGB-3 (у 36 по гетерозиготной аллели и у 3 – по гомозиготной). Эффективность ВРТ у 38 пациенток была положительной (из них 10 в гетерозиготной аллели, а у 1– в гомозиготной). Эффективность ВРТ отрицательна у 23 пациенток (из них в гетерозиготной аллели находился мутировавший ген у 19 пациенток, а в гомозиготной – у 4).
В 35,4% случаев (39 пациенток) наблюдалась мутация в гене FGB (8 – по гомозиготной аллели, 31 – по гетерозиготной). Эффективность ВРТ у 48 пациенток была положительной (из них у 8 мутированный ген FGB находился в гетерозиготной аллели, а у 4 – в гомозиготной). ВРТ отрицательно у 21 пациентки (мутация в гетерозиготной аллели – 17 случаев, у 4 – в гомозиготной аллели).
В 60,9% случаев (67 пациенток) наблюдалась мутация в гене F13 (в 12 случаях – гомозиготная аллель, 55 – гетерозиготная). Эффективность ВРТ у 48 пациенток была положительной. Из них у 12 пациенток мутированный ген F13 находился в гетерозиготной аллели, а у 4 – в гомозиготной аллели. ВРТ отрицательно у 39 пациенток. При этом гомозиготная аллель наблюдалась в 8 случаях, а гетерозиготная аллель – в 31.
В 30 случаях (27,2%) наблюдалась мутация в гене F7. Преимущественно по гетерозиготной аллели – 28 пациенток, а гомозиготная аллель обнаружена у 2. При этом беременность наступила у 8 пациенток, причем у всех мутированный ген F7 находился в гетерозиготной аллели. Беременность не наступила у женщин, имеющих мутацию в гомозиготной аллели.
У 5 пациенток (4,5% случаев) наблюдалась мутация в гене F5 (мутация Лейдена). При этом во всех случаях беременность не наступила.
В 5 случаях так же наблюдалась мутация в гене MTHRR-98 в гетерозиготной аллели. ВРТ была положительной у 2 пациенток.
У 12 пациенток (10,9%) наблюдалась мутация в гене MTHRR-66. Гомозиготная аллель обнаружена в 3 случаях, гетерозиготная аллель – в 9. Эффективность ВРТ была обнаружена лишь у 5 пациенток, из которых у 4 пациенток мутированный ген находился в гетерозиготной аллели, а у 1 – в гомозиготной аллели.
У 5 пациенток(4,5%) наблюдалась мутация в гене MTHRR-56. Гомозиготная аллель обнаружена в 4 случаях, гетерозиготная аллель – 1. Эффективность ВРТ положительна у 1 пациентки (мутированный ген в гетерозиготной аллели). (См. рис. 3,4)
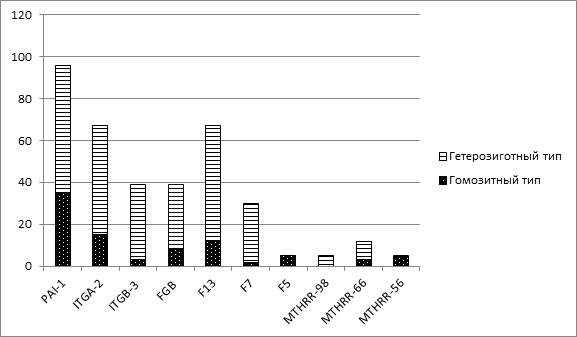
Рис. 3. Распределение генных мутаций среди пациенток с бесплодием.
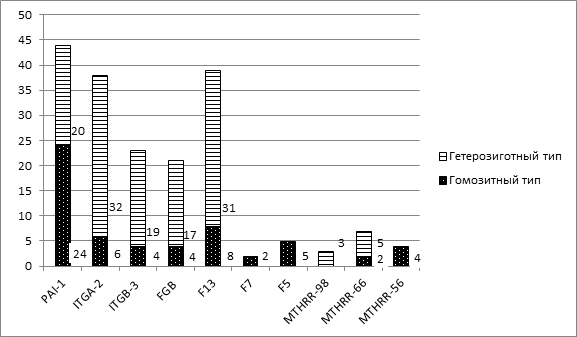
Рис. 4. Распределение генных мутаций среди пациенток с бесплодием по количеству отрицательных результатов ВРТ (абсолютные показатели).
У женщин с ПНБ 32 (100%) встречались мутации в гене F2 по гетерозиготному типу в 1 случае; мутация гена F5 (лейденский фактор) – 3 (в 2 случаях по гомозиготному типу и в 1 – по гетерозиготному); мутация гена F7 – 7 (22%) из них в 1случае по гомозиготному типу и в 6 – по гетерозиготному; в генах F13 – 10 (31,3%) из них в 9 случаях по гетерозиготному типу и в 1 – по гомозиготному; мутация в гене FGB -12 (44%) из них в 11 по гетерозиготному типу и в 1 – по гомозиготному; мутация в гене ITGA2 -18 (56,3%) из них в 4 по гомозиготному и 14 по гетерозиготному типам; мутация гена ITGB3 – 10 (31,3%) все мутации встречались по гетерозиготному типу; мутация в гене SERPINE1 – 19 (59,4%) из них в 15 случаях по гетерозиготному типу и 4 случая по гомозиготному типу; мутация MTHFR677 8(25%)случаях из них в 7 случаях по гетерозиготному типу и 1 – по гомозиготному типу; мутация MTHFR 1298 в 10 случаях по гетеро- и гомозиготному типу в 5 случаях; мутация в гене MTR 6(19%) из них все по гетерозиготному типу и мутация в гене MTRR в 14(44%)случаях из них в 6 случаях по гомозиготному типу и 8 по гетерозиготному типу. У всех 32(100%) пациенток имела место быть комбинированная форма тромбофилии. (См. рис. 5)
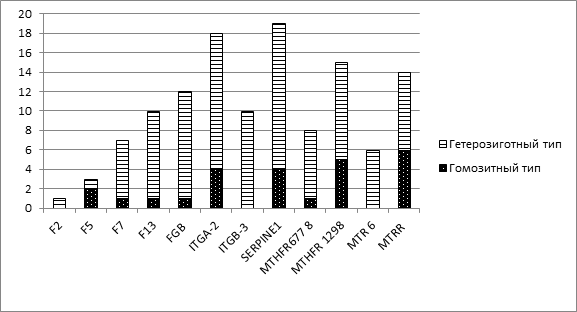
Рис. 5. Струтура генных мутаций среди пациенток с ПНБ.
Таким образом, по результатам предварительных исследований можно сделать следующие выводы: Мутация гена PAI-1 в гомозиготном варианте в 21,8% случаях сопровождается отрицательным результатом применения ВРТ при бесплодии у женщин, что связанно с более высокой склонностью к тромбообразованию (нарушению функции эндотелия, усиление коагуляционного и снижение антикоагуляционного потенциала). Последующее формирование микротромбов приводит к сосудистому отторжению эмбриона. Мутации в других генах, таких как F13, FGB, ITGA-2, ITGA-3, сопровождалось отрицательными результатами ВРТ преимущественно в гетерозиготных аллелях; а F5, F7, MTHRR-56 – в гомозиготных.
У женщин с репродуктивными потерями, обусловленными невынашиванием беременности, выявлена высокая частота генетических тромботических дефектов и их ассоциаций. Определен высокий удельный вес носительства полиморфизма генов PAI-1 (59,4%), а так же ITGA-2 (56,3%); мутация в гене FGB – 44% и MTHFR 31,2% случаях. У всех 32 пациенток имела место быть комбинированная форма тромбофилии.
Раннее выявление этих генетических аномалий является обязательным для женщин фертильного возраста, так как дает возможность своевременно назначить адекватную терапию и предотвратить возможные репродуктивные потери. Правильно собранный анамнез у женщин перед планированием беременности дает новые возможности к формированию групп риска по невынашиванию беременности и по тромбоэмболическим осложнениям.
Пациенткам, имеющим генетически обусловленные факторы тромбогенного риска, показано динамическое исследование системы гемостаза с определением уровня маркеров тромбинемии (растворимый фибрин, D-димер), функциональной активности тромбоцитов.
Но по Приказу Министерства здравоохранения РФ от 1 ноября 2012 г. № 572н “Об утверждении Порядка оказания медицинской помощи по профилю «акушерство и гинекология (за исключением использования вспомогательных репродуктивных технологий)»” (ист.: ГАРАНТ) нет рекомендаций о том, что у женщин с высоким тромбогенным риском необходимо определять гомоцистеин и D-димер. Данный регламент при включении его в стандарты в свою очередь помог бы в своевременном выявлении изменений в системе гемостаза и назначении дальнейшей адекватной терапии (витамины гр.В, антикоагулянты, НМГ), повышая тем самым процент вынашивания беременности и положительный результат программы ВРТ при бесплодии. Так же необходимо включить в рекомендации консультацию гематолога для женщин с выявленными генетическими тромбофилиями на этапе предгравидарной подготовки.
Библиографический список
- Бицадзе В.О., Акиньшина С.В., Макацария А.Д., Андреева М.Д. Вспомогательные репродуктивные технологии и ятрогенные тромботические осложнения // Вопросы гинекологии, акушерства и перинатологии. – 2014. – №1. – С. 49-59.
- Activation of coagulation in amniotic fluid during normal human pregnancy – [Электронный ресурс ] – // ncbi.nlm.nih.gov: U.S. National Library of Medicine 2011 URL: https://www.ncbi.nlm.nih.gov/pubmed/21504838 (дата обращения: 14.01.17).
- McLean K.C., Bernstein I.M., Brummel-Ziedins K.E. Tissue factor-dependent thrombin generation across pregnancy // American Journal of Obstetrics & Gynecology. – 2012. – №207(2).
- Kamel H., Navi B.B., Sriram N., Hovsepian D.A., Devereux R.B., Elkind M.S. Risk of a thrombotic event after the 6-week postpartum period // New England Journal of Medicine. – 2014. – №370. – С. 307-315.
- Thrombophilia and Pregnancy Complications – [Электронный ресурс ] –// ncbi.nlm.nih.gov: U.S. National Library of Medicine 2015 URL: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4691051/ (дата обращения: 11.01.2016).
- Thrombophilic genes alterations as risk factor for recurrent pregnancy loss – [Электронный ресурс ] – // ncbi.nlm.nih.gov: U.S. National Library of Medicine 2016 URL: https://www.ncbi.nlm.nih.gov/pubmed/26135458 (дата обращения: 7.01.2017).
- Тромбофилия как причина акушерских осложнений – [Электронный ресурс ] – // http://internist.ru: Всероссийская образовательная интернет-программа для врачей 2014 URL: http://internist.ru/publications/detail/7185/ (дата обращения: 12.01.2017).
Количество просмотров публикации: Please wait


